മരുന്നുകളുടെ പ്രിയപ്പെട്ട സബ് സെല്ലുലാർ വേട്ടകൾ പ്രവചിക്കാൻ മെഷീൻ ലേണിംഗ് സഹായിക്കുന്നു
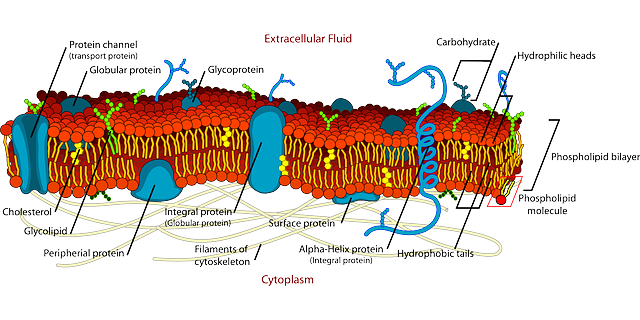
മിക്ക മരുന്നുകളും പ്രവർത്തിക്കുന്നതിനായി ഒരു നിർദ്ദിഷ്ട ലക്ഷ്യവുമായി ഉറച്ചുനിൽക്കുന്ന ചെറിയ തന്മാത്രകളാണ് – ഒരു രോഗത്തിൽ ഉൾപ്പെട്ടിരിക്കുന്ന മനുഷ്യ കോശങ്ങളിലെ ചില തന്മാത്രകൾ. ഉദാഹരണത്തിന്, ഒരു കാൻസർ മരുന്നിന്റെ ലക്ഷ്യം കാൻസർ കോശങ്ങൾക്കുള്ളിൽ സമൃദ്ധമായ ഒരു തന്മാത്രയായിരിക്കാം. മരുന്ന് അതിന്റെ ലക്ഷ്യത്തിലെത്തുന്നതുവരെ കോശത്തിലുടനീളം സ്വതന്ത്രമായി സഞ്ചരിക്കുകയും തുടർന്ന് അതിൽ ലോക്ക് ചെയ്യുകയും വേണം, ഇത് ഒരു ചികിത്സാ പ്രവർത്തനത്തിലേക്ക് നയിക്കുന്നു.
എന്നിരുന്നാലും, ചെറിയ തന്മാത്രാ മരുന്നുകൾ അത്തരം അനിയന്ത്രിതമായ രീതിയിൽ സഞ്ചരിക്കുന്നില്ല; പകരം, അവ കോശത്തിന്റെ നിർദ്ദിഷ്ട പ്രദേശങ്ങളിൽ ശ്രദ്ധ കേന്ദ്രീകരിക്കുന്നു. കാരണം, ഓരോ മരുന്നിനും അതിന്റെ ലക്ഷ്യത്തേക്കാൾ കൂടുതൽ തന്മാത്രകളുമായി സംവദിക്കാൻ കഴിയും.
ഈ മറ്റ് പ്രതിപ്രവർത്തനങ്ങൾ ദുർബലമാണ്, സ്റ്റാറ്റിക് ക്ലിംഗ്, ശക്തമായ കാന്തത്തിന്റെ വലിക്കൽ എന്നിവ പോലെ, പക്ഷേ തന്മാത്രകൾ കണ്ടൻസേറ്റുകൾ എന്നറിയപ്പെടുന്ന സെല്ലുലാർ കമ്പാർട്ടുമെന്റുകളിൽ ഒരുമിച്ച് കേന്ദ്രീകരിക്കുമ്പോൾ അവ ശേഖരിക്കാൻ കഴിയും. ഈ കമ്പാർട്ടുമെന്റുകളിൽ, കൂട്ടായ ദുർബലമായ ഇടപെടലുകൾ മയക്കുമരുന്ന് തന്മാത്രകളുടെ ഗണ്യമായ ഒരു ശതമാനം തടഞ്ഞുവച്ചേക്കാം, അവയെ അവരുടെ ലക്ഷ്യത്തിന്റെ അതേ അയൽപക്കത്തോ അതിൽ നിന്ന് വളരെ അകലെയോ പ്രാദേശികവൽക്കരിച്ചേക്കാം.
വൈറ്റ്ഹെഡ് ഇൻസ്റ്റിറ്റ്യൂട്ട് അംഗം റിച്ചാർഡ് യങ്ങിന്റെ ലാബിലെ ഗവേഷകർ വ്യത്യസ്ത കണ്ടൻസേറ്റുകളുടെ ഉള്ളിലെ രാസ പരിതസ്ഥിതികളും ഈ രസതന്ത്രങ്ങൾ ചെറിയ തന്മാത്രകളുമായി എങ്ങനെ ഇടപെടുന്നുവെന്നും മനസിലാക്കാൻ പ്രവർത്തിക്കുന്നു. സെപ്റ്റംബർ 28 ന് നേച്ചർ കെമിക്കൽ ബയോളജിയിൽ പ്രസിദ്ധീകരിച്ച ഗവേഷണത്തിൽ, മസാച്ചുസെറ്റ്സ് ഇൻസ്റ്റിറ്റ്യൂട്ട് ഓഫ് ടെക്നോളജിയിലെ (എംഐടി) കമ്പ്യൂട്ടർ സയൻസ് & ആർട്ടിഫിഷ്യൽ ഇന്റലിജൻസ് ലാബിലെ ആർട്ടിഫിഷ്യൽ ഇന്റലിജൻസ് ആൻഡ് ഹെൽത്ത് സ്കൂൾ ഓഫ് എഞ്ചിനീയറിംഗ് വിശിഷ്ട പ്രൊഫസർ റെജീന ബാർസിലേ ഉൾപ്പെടെയുള്ള യങ്ങും സഹപ്രവർത്തകരും ഒരു മെഷീൻ ലേണിംഗ് മോഡൽ പരിശീലിപ്പിച്ചു.
കണ്ടൻസേറ്റുകളും ചെറിയ തന്മാത്രകളും തമ്മിലുള്ള പ്രതിപ്രവർത്തനങ്ങൾ കോശത്തിൽ ഒരു ചെറിയ തന്മാത്ര എവിടെ അവസാനിക്കുമെന്നും അത് എന്തുമായി ഇടപഴകുമെന്നും നിർണ്ണയിക്കാൻ സഹായിക്കുന്നു, ഇത് പല സെല്ലുലാർ പ്രക്രിയകളും മനസിലാക്കുന്നതിനും സുരക്ഷിതവും ഫലപ്രദവുമായ മരുന്നുകളുടെ രൂപകൽപ്പനയ്ക്കും പ്രസക്തമായിരിക്കാം.
ഉദാഹരണത്തിന്, ഒരു ചെറിയ തന്മാത്ര മരുന്നിന്റെ ഒരു വലിയ ശതമാനം മരുന്നിന്റെ ലക്ഷ്യം അടങ്ങിയിട്ടില്ലാത്ത ഒരു കണ്ടൻസേറ്റിൽ അവസാനിക്കുകയാണെങ്കിൽ, അത് പ്രവർത്തിക്കുന്നതിന് മരുന്നിന്റെ ഉയർന്ന ഡോസുകൾ ആവശ്യമായി വന്നേക്കാം, ഇത് വിഷാംശത്തിന്റെയും അപ്രതീക്ഷിത പാർശ്വഫലങ്ങളുടെയും സാധ്യത വർദ്ധിപ്പിക്കുന്നു. നേരെമറിച്ച്, അതേ കണ്ടൻസേറ്റ് പതിവായി ഉപയോഗിക്കാൻ രൂപകൽപ്പന ചെയ്ത ഒരു മരുന്ന് കുറഞ്ഞ അളവിൽ കൂടുതൽ ഫലപ്രദമായിരിക്കും – അതിനാൽ, സാധാരണയായി, സുരക്ഷിതമായ- ഡോസുകളിൽ.
“വളരെ ഫലപ്രദമായ ഒരു മരുന്ന് വികസിപ്പിക്കാൻ നിങ്ങൾ ആഗ്രഹിക്കുന്നുവെങ്കിൽ, ഈ കമ്പാർട്ടുമെന്റുകളുമായി ബന്ധപ്പെട്ട് കോശത്തിൽ മരുന്നിന്റെ ലക്ഷ്യം എവിടെയാണെന്ന് നിങ്ങൾ അറിഞ്ഞിരിക്കണമെന്ന് ഞങ്ങളുടെ പഠനം സൂചിപ്പിക്കുന്നു,” എംഐടിയിലെ ബയോളജി പ്രൊഫസർ കൂടിയായ യംഗ് പറയുന്നു. “ഒരു മരുന്ന് വികസിപ്പിക്കാനുള്ള ഏറ്റവും മികച്ച മാർഗത്തെക്കുറിച്ച് ഇത് ഗവേഷകരെയും കമ്പനികളെയും അറിയിക്കും, അതുവഴി അത് അതിന്റെ ലക്ഷ്യത്തിനടുത്ത് മികച്ച രീതിയിൽ കേന്ദ്രീകരിക്കപ്പെടും.”
ഡീകോഡിംഗ് കണ്ടെൻസേറ്റ് കെമിസ്ട്രി
ചില തന്മാത്രകൾ ഒരുമിച്ചുചേർന്ന് കോശത്തിനുള്ളിൽ ഒരു തുള്ളി ഉണ്ടാക്കുമ്പോൾ രൂപപ്പെടുന്ന കണ്ടൻസേറ്റുകൾ, മെംബ്രൻ-ലെസ് സെല്ലുലാർ കമ്പാർട്ടുമെന്റുകൾ എന്നിവയെക്കുറിച്ചുള്ള പഠനത്തിനായി യുവ ലാബ് ഗവേഷകർ വർഷങ്ങളോളം ചെലവഴിച്ചു. ഈ തുള്ളികൾ സംഘടനാ ഇടങ്ങളായി പ്രവർത്തിക്കുന്നു, അതിൽ കോശത്തിന് അവയുടെ പ്രവർത്തനങ്ങൾ നിർവഹിക്കുന്നതിന് ശരിയായ സ്ഥലത്ത് തന്മാത്രകളുടെ ശരിയായ സംയോജനം ശേഖരിക്കാൻ കഴിയും.
വ്യത്യസ്ത സെല്ലുലാർ പ്രക്രിയകളിൽ കണ്ടൻസേറ്റുകൾ ഈ സംഘടനാപരമായ പങ്ക് വഹിക്കുന്നുവെന്നതിന് യുവാക്കളും മറ്റുള്ളവരും തെളിവുകൾ കണ്ടെത്തിയിട്ടുണ്ട്. മരുന്നുകൾക്ക് കണ്ടൻസേറ്റുകളിൽ ശ്രദ്ധ കേന്ദ്രീകരിക്കാൻ കഴിയുമെന്നും ഇത് അവയുടെ ഫലപ്രാപ്തിയെ ബാധിച്ചേക്കാമെന്നും അവർ തെളിവുകൾ കണ്ടെത്തി. സാധാരണയായി ഉപയോഗിക്കുന്ന കാൻസർ മരുന്നായ സിസ്പ്ലാറ്റിൻ ട്രാൻസ്ക്രിപ്ഷണൽ കണ്ടൻസേറ്റുകളിൽ ശ്രദ്ധ കേന്ദ്രീകരിക്കുന്നുവെന്ന് കാണിക്കുന്ന ഒരു സയൻസ് പേപ്പർ 2020 ൽ യങ്ങും സഹപ്രവർത്തകരും പ്രസിദ്ധീകരിച്ചു.
പുതിയ പ്രബന്ധത്തിന്റെ സഹ-രചയിതാക്കളായ യുവ ലാബ് പോസ്റ്റ്ഡോക്ടർ ഹെൻറി കിൽഗോറും ബിരുദ വിദ്യാർത്ഥി കലോൺ ഓവർഹോൾട്ടും വ്യത്യസ്ത മരുന്നുകൾ വ്യത്യസ്ത കണ്ടൻസേറ്റുകളിൽ എങ്ങനെ കേന്ദ്രീകരിക്കുന്നുവെന്ന് ആസൂത്രിതമായി പരീക്ഷിച്ചാൽ തങ്ങൾ എന്തു പഠിക്കുമെന്ന് ആശ്ചര്യപ്പെട്ടു. ഒന്നാമതായി, മുഴുവൻ കോശത്തിലുടനീളം സ്വതന്ത്രമായി ചിതറിപ്പോകുന്നതിനുപകരം മരുന്നുകൾ നിർദ്ദിഷ്ട കമ്പാർട്ടുമെന്റുകളിൽ ശ്രദ്ധ കേന്ദ്രീകരിക്കുന്നത് ഒരു സാധാരണ സംഭവമാണെന്ന് സ്ഥിരീകരിക്കാൻ അവർ മരുന്നുകളുടെ ഒരു വലിയ ശേഖരം പരീക്ഷിച്ചു: അത് ഉണ്ടെന്ന് അവർ കണ്ടെത്തി.
അടുത്തതായി, മരുന്നുകൾ ഒരു കണ്ടൻസേറ്റിൽ മറ്റൊന്നിന് മുകളിൽ കേന്ദ്രീകരിക്കാൻ കാരണമാകുന്നത് എന്താണെന്ന് പഠിക്കാൻ അവർ ഒരു സംവിധാനം ആവിഷ്കരിച്ചു. അവർ മൂന്ന് പ്രധാന തരം കണ്ടൻസേറ്റുകളുടെ മാതൃകകൾ സൃഷ്ടിച്ചു: ഒന്ന് ജീൻ ട്രാൻസ്ക്രിപ്ഷനിൽ ഉൾപ്പെടുന്നു, ഒന്ന് ജീൻ അടിച്ചമർത്തലിൽ ഉൾപ്പെടുന്നു, റൈബോസോമുകൾ ഉത്പാദിപ്പിക്കുന്ന ന്യൂക്ലിയസിനുള്ളിലെ ഒരു വലിയ കണ്ടൻസേറ്റ്. ഗവേഷകർ ഈ മൂന്ന് തരം കണ്ടൻസേറ്റുകളുടെ ചട്ടക്കൂട് രൂപപ്പെടുത്തുന്ന പ്രബലമായ തരം പ്രോട്ടീൻ വേർതിരിച്ചെടുക്കുകയും ഓരോ പ്രബല പ്രോട്ടീനും മാത്രം നിർമ്മിച്ച ലളിതമായ കണ്ടൻസേറ്റുകൾ രൂപീകരിക്കുകയും ചെയ്തു.
തുടർന്ന് ഗവേഷകർ വൈവിധ്യമാർന്ന രാസ സവിശേഷതകളുള്ള 1,500 ലധികം ചെറിയ തന്മാത്രകളുടെ ഒരു ലൈബ്രറി സമാഹരിക്കുകയും മൂന്ന് മോഡൽ കണ്ടൻസേറ്റുകളിൽ ഓരോന്നിലും അവ എത്ര ശക്തമായി കേന്ദ്രീകരിക്കുമെന്ന് പരിശോധിക്കുകയും ചെയ്തു. ചെറിയ തന്മാത്രകളിൽ ഭൂരിഭാഗവും മറ്റുള്ളവയേക്കാൾ ഒരു ഘനീഭവനത്തെ അനുകൂലിച്ചു. ബാർസിലേയുടെ ലാബിലെ ബിരുദ വിദ്യാർത്ഥിയായ സഹ-ആദ്യ രചയിതാവ് പീറ്റർ മിഖായേൽ, ചെറിയ തന്മാത്രകൾ വ്യത്യസ്ത കണ്ടൻസേറ്റുകളായി തരംതിരിക്കുന്ന രീതികളിലെ പാറ്റേണുകൾ തിരിച്ചറിയാൻ ഈ ഡാറ്റയിൽ ഒരു മെഷീൻ ലേണിംഗ് മോഡൽ പരിശീലിപ്പിച്ചു.
ഓരോ തരം കണ്ടൻസേറ്റിനെയും അനുകൂലിക്കുന്ന തന്മാത്രകൾക്ക് പങ്കിട്ട രാസ സവിശേഷതകൾ ഉണ്ടെന്നും മറ്റ് കണ്ടൻസേറ്റ് തരങ്ങളെ അനുകൂലിക്കുന്ന തന്മാത്രകളേക്കാൾ പരസ്പരം സമാനമാണെന്നും മോഡൽ കണ്ടെത്തി. തന്മാത്രകൾ എവിടെ അവസാനിക്കുന്നു എന്നതിനെ ബാധിക്കുന്നതായി തോന്നുന്ന നിരവധി സവിശേഷതകൾ ഇത് തിരിച്ചറിഞ്ഞു. ഉദാഹരണത്തിന്, ട്രാൻസ്ക്രിപ്ഷണൽ കണ്ടൻസേറ്റുകൾ ഇലക്ട്രോൺ സമ്പന്നമായ സുഗന്ധ വളയങ്ങൾ (ഒരു പ്രത്യേക തരം വളയ ഘടന) അടങ്ങിയ ചെറിയ തന്മാത്രകളെ ആകർഷിക്കുന്നു. ഈ പാറ്റേണുകൾ ഉപയോഗിച്ച്, ലളിതമായ കണ്ടൻസേറ്റുകളിൽ ഏതിൽ കൂടുതൽ മരുന്നുകൾ കേന്ദ്രീകരിക്കുമെന്ന് പ്രവചിക്കുന്നതിൽ മോഡൽ വളരെ മികച്ചതായിരുന്നു.
അടുത്തതായി, ജീവനുള്ള കോശങ്ങളിൽ മരുന്നുകൾ എവിടെ കേന്ദ്രീകരിക്കുമെന്ന് മോഡലിന് എത്ര നന്നായി പ്രവചിക്കാൻ കഴിയുമെന്ന് ഗവേഷകർ പരീക്ഷിച്ചു. ഇത് മിതമായ വിജയം നേടി. സിംഗിൾ-പ്രോട്ടീൻ കണ്ടൻസേറ്റുകളുടെ ലളിതമായ കേസുകളിൽ മോഡൽ പരിശീലനം നൽകിയതായി കുറഞ്ഞ കൃത്യത പ്രതിഫലിപ്പിക്കുന്നു. ഒരു കോശത്തിൽ, കണ്ടൻസേറ്റുകളിൽ നൂറുകണക്കിന് പ്രോട്ടീനുകൾ അടങ്ങിയിരിക്കുന്നു, അവ ഓരോന്നും പ്രാദേശിക രാസ പരിതസ്ഥിതിയെ സ്വാധീനിച്ചേക്കാം, കൂടാതെ കണ്ടൻസേറ്റുകളും മറ്റ് സെല്ലുലാർ കമ്പാർട്ടുമെന്റുകളും ഒറ്റപ്പെട്ട് നിലവിലില്ല: അവ ഒരു മരുന്ന് ശേഖരിക്കാൻ മത്സരിക്കുന്നു.
ഈ നിരവധി പ്രോട്ടീനുകളുടെ ഭൗതികവും രാസപരവുമായ ഗുണങ്ങൾ മനസിലാക്കാൻ ഗവേഷകർ ഇപ്പോൾ പ്രവർത്തിക്കുന്നു, അതുവഴി അവർക്ക് അവരുടെ മോഡലുകൾ മെച്ചപ്പെടുത്താൻ കഴിയും. കണ്ടൻസേറ്റുകൾ ചില തന്മാത്രകൾക്ക് മറ്റുള്ളവയേക്കാൾ അനുകൂലമായ രാസാന്തരീക്ഷം സൃഷ്ടിക്കുന്ന നിർദ്ദിഷ്ട സംവിധാനങ്ങളെക്കുറിച്ച് ചുരുക്കാനും അവർ ഉദ്ദേശിക്കുന്നു.
“കണ്ടൻസേറ്റ് ബയോകെമിസ്ട്രി ഉപയോഗിക്കുന്നതിന്, വ്യത്യസ്ത തന്മാത്രകൾ എവിടെയാണ് കേന്ദ്രീകരിക്കുന്നത് എന്നതിനെക്കുറിച്ച് പ്രവചന ശക്തി ഉണ്ടായിരിക്കാൻ ഞങ്ങൾ ആഗ്രഹിക്കുന്നു. ഞങ്ങൾ ഇപ്പോഴും പ്രാരംഭ ഘട്ടത്തിലാണെങ്കിലും, ഞങ്ങൾ സമന്വയിപ്പിക്കുന്ന മരുന്നുകൾ കൃത്യമായി എവിടെ പോകുമെന്നതിനെക്കുറിച്ച് ഞങ്ങൾക്ക് മികച്ച നിയന്ത്രണമുള്ള ഒരു ലോകം വിഭാവനം ചെയ്യുന്നത് ആവേശകരമാണ്, അതായത് അവയ്ക്ക് പരമാവധി ഫലപ്രാപ്തിയും അനാവശ്യ പാർശ്വഫലങ്ങളും കുറവാണ്,” മിഖായേൽ പറയുന്നു.
അതേസമയം, കോശങ്ങൾ എങ്ങനെ സംഘടിപ്പിക്കപ്പെടുന്നുവെന്ന് പുനർവിചിന്തനം ചെയ്യേണ്ടതിന്റെയും തന്മാത്രകൾ അവയുടെ രാസ സവിശേഷതകളെ അടിസ്ഥാനമാക്കി എവിടെ കേന്ദ്രീകരിക്കുന്നുവെന്ന് പരിഗണിക്കുന്നതിന്റെയും പ്രാധാന്യം ഈ കൃതി പ്രകടമാക്കുന്നുവെന്ന് ഗവേഷകർ പ്രതീക്ഷിക്കുന്നു.
“കോശത്തിന്റെ ഉൾഭാഗം വളരെ കംപാർട്ട്മെന്റലൈസ്ഡ് ആയി പരിണമിച്ചു, അതിനർത്ഥം കോശത്തിനുള്ളിലെ ചെറിയ തന്മാത്രകൾ ഏകീകൃതമായി വിതരണം ചെയ്യപ്പെടുന്നില്ല എന്നാണ്,” ഓവർഹോൾട്ട് പറയുന്നു. “വിവിധ മേഖലകളിൽ നിന്നുള്ള വിദഗ്ധരുമായി സംസാരിക്കുന്നതും കോശത്തിൽ തന്മാത്രകൾ യഥാർത്ഥത്തിൽ എങ്ങനെ വിതരണം ചെയ്യുന്നു എന്നതിനെക്കുറിച്ചുള്ള ഞങ്ങളുടെ പ്രവർത്തനത്തിൽ നിന്ന് എത്ര ശാഖകൾ നേടാൻ കഴിയുമെന്ന് മനസ്സിലാക്കുന്നതും ആവേശകരമാണ്.”
മരുന്ന് ഡെവലപ്പർമാർക്ക് അവരുടെ പ്രവർത്തനം വളരെ ഉപയോഗപ്രദമാകുമെന്ന് ഗവേഷകർ പ്രതീക്ഷിക്കുന്നു, പക്ഷേ കോശങ്ങൾക്കുള്ളിൽ സംഭവിക്കുന്ന മറ്റ് നിരവധി പ്രക്രിയകൾക്ക് ഇത് പ്രസക്തമാണെന്ന് തെളിയിക്കുമെന്നും അവർ പ്രതീക്ഷിക്കുന്നു. പ്രസക്തമായ തന്മാത്രകൾ എപ്പോൾ, എവിടെ കേന്ദ്രീകരിക്കുന്നുവെന്ന് ക്രമീകരിക്കുന്നതിന് കൂടുതൽ നിർണായക സെല്ലുലാർ പ്രക്രിയകൾ കണ്ടൻസേറ്റുകളെ ആശ്രയിക്കുന്നതായി കണ്ടെത്തി. ഈ ഓർഗനൈസേഷനെ നിയന്ത്രിക്കുന്ന കെമിക്കൽ കോഡിംഗ് ഗവേഷകർ നന്നായി മനസ്സിലാക്കുന്നു, അവശ്യ സെല്ലുലാർ പ്രക്രിയകൾ എങ്ങനെ നടക്കുന്നുവെന്നും രോഗത്തിൽ അവയുമായി എന്താണ് സംഭവിക്കുന്നതെന്നും അവർ നന്നായി മനസ്സിലാക്കും.
“ഈ പഠനത്തിൽ കണ്ടൻസേറ്റുകളെക്കുറിച്ച് ഞങ്ങൾ പഠിച്ചതെല്ലാം സൂചിപ്പിക്കുന്നത് കണ്ടൻസേറ്റുകളും മറ്റ് സെല്ലുലാർ അവയവങ്ങളും ചെറിയ തന്മാത്രകളുടെ വിതരണത്തിൽ ശക്തമായ സ്വാധീനം ചെലുത്തുന്നുവെന്നാണ്,” കിൽഗോർ പറയുന്നു. “കണ്ടൻസേറ്റ് ചെറിയ തന്മാത്ര സെലക്ടിവിറ്റിക്ക് ജീവശാസ്ത്രത്തിനും മരുന്ന് കണ്ടെത്തലിനും അടിസ്ഥാനപരമായ പ്രത്യാഘാതങ്ങളുണ്ടെന്ന് എനിക്ക് ഈ ഘട്ടത്തിൽ ബോധ്യമുണ്ട്.”
Experienced Researcher with a demonstrated history of working in the Deep Learning, Computer Vision